Dr. Cihan Taştan
Hedef Doku ve Hücrelere Gen Terapi Sistemlerinin Taşıma Teknolojileri
TALEN’lerin (Transcription activator like effector nuclease) ve FN’lerin (Zinc-finger nuclease) yanı sıra CRISPR-Cas9'a dayanan genom modifikasyon sistemleri, iyomedikal araştırma, ilaç keşfi ve geliştirme, hatta gen terapisi için değerli teknolojiler olmaya başladı.
Bununla birlikte, bu sistemlerin her biri hücrelere etkili bir şekilde girebilmek ve işlevlerini yerine getirebilmek için verimli ve güvenli taşıma teknolojilerine ihtiyaç duyuyor. Gen terapilerinde hücre içerisine bu makromoleküllerin taşınması veya enjekte edilebilmesi için viral ve viral olmayan paketleme yöntemleri üzerinde çalışmalar olanca hızıyla devam ediyor.
7000 tespit edilmiş nadir hastalıkların sadece %5'ten azı için etkili bir tedaviye sahip olduğumuz düşünüldüğünde, gen terapi yöntemlerine olan ihtiyacın ne denli yüksek olduğu tartışılmazdır. Genetik hastalıklara sebep olan mutasyona uğramış genlerin, fonksiyonel kopyalarının viral veya viral-olmayan sistemlerle hücre içine transferi ile fonksiyon kaybının giderilebilmesi, gen terapilerinin önemini ortaya koydu. 2012 yılında, nadir hastalıklardan lipoprotein lipaz eksikliğini tedavi etmek için adenoilişkili virüs (AAV) aracılı fonksiyonel bir genin aktarılması, viral gen aktarım teknolojisine dayanan ilk gen terapisinin ürünü oldu.
Ayrıca, hastalık genlerinden üretilen mRNA'ları sessizleştiren RNAi (RNA interference) ve ASO (antisense oligonükleotidler) gibi RNA modifikasyon terapileri de şu an üzerinde klinik araştırmalar gerçekleştirilen diğer terapi yöntemlerinden birkaçı. ASO'lar ve RNAi, herhangi bir hedef proteinin üretiminin baskılanmasına neden olabilir. Yine de hastalık proteinlerinin
tamamen değil; sadece bir seviyeye kadar baskılanabilmesi ve hedef dışı etkiler, RNA ile modifikasyon terapilerinin dezavantajlarının olduğunu gösteriyor.
Adeno-ilişkili virüs (AAV) aracılı gen terapi moleküllerinin taşınması, bölünmeyen hücrelerde gen transferi ve episomal ifadeyi kolaylaştırır. Ancak kapsüllenmiş gen terapi moleküllerinin
boyutu ve AAV vektörlerine karşı vücudumuzun verdiği bağışıklık tepkisi, gen terapilerinde AAV teknolojisinin kullanılmasında da zorluklar yaşanabildiğini gösteriyor.
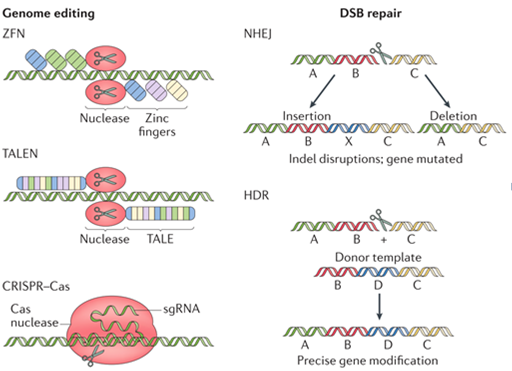
İnsan hücrelerinde gen ekspresyonunu manipüle etmek için geliştirilen alternatif bir teknoloji de programlanabilir DNA nükleaz’larıdır. ZFN, TALEN ve CRISPR-Cas9 nukleaz tabanlı sistemler, DNA'da çift sarmal kırılmalarını (DSB'ler) indükleyebilir. Çift DNA sarmalı kırılmaları, hücreyi genom düzenlemeye iki yolla zorlar: Homolog olmayan son katılım (NHEJ) ve homoloji yöneltilmiş onarım (HDR). NHEJ, hedef gen eklenmesi (insertion) veya silinmesi amacıyla DNA’nın belirli bölgesini parçalarken; HDR, genomik dizilerin eklenmesi, silinmesi veya değiştirilmesi için hedef genomik bölgeye donör DNA parçacığının eklenmesine olanak sunar. HDR'ye dayalı gen düzenleme yöntemi, hastalık nedenli mutasyonları onarmak için kullanılabilmekte.
Bu genetik düzenleme teknolojileri ile birçok genetik hastalığı düzeltmek artık mümkün. Bununla birlikte, bu muazzam terapötik potansiyeli gerçekleştirmek için, hücre içerisine güvenli ve verimli olarak transfer edilmesi noktasında birçok engelin aşılması gerekiyor.
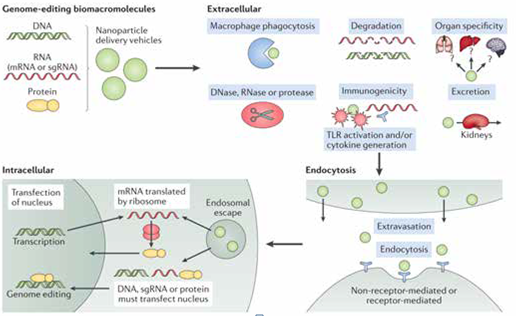
Genom düzenleme sistemlerinde yer alan tüm bileşenler, hedef hücrelerde işlev görmesi için DNA, mRNA veya protein biçiminde hedef hücrelerin genomuna erişmelidir. Genom düzenleme makromolekülleri içeren nanoparçacıklar, öncelikle hücre dışı engellerden kaçınmalıdır.
Bu bariyerler, makrofajlar veya diğer fagositler tarafından fagositoz, enzimatik veya hidrolitik yollarla bozunum, bağışıklık tepkisinin indüklenmesi ve sitokinlerin üretilmesi. Eğer bu makromoleküller ve nanoparçacıklar bahsettiğimiz bariyerlerden kaçınabilir, doğru organa lokalize olur ve kan dolaşımından sızarsa hedef hücre tarafından içeriye alınır. Böylelikle, hedef geni başarıyla düzenleyebilmek için sitoplazmaya (mRNA) veya çekirdeğe (DNA, sgRNA veya nükleaz proteini) lokalize olmaları yeterli olacaktır.
Genellikle incelenen, genetik materyali terapötik olarak kullanılmak üzere tasarlanan üç virüs sınıfı vardır: retrovirüsler, adenovirüsler ve adenoilişkili virüsler (AAV'ler). Bunlara alternatif olarak, viral olmayan materyallere dayalı gönderim vektörleri viral vektörlerden daha az toksik ve immünojenik olma potansiyeline sahiptir.
Nükleik asitlerin hücre içerisine verimli transferi için ayrıca sentetik polimerler (örneğin polietilenimin, siklodekstrin ve p-amino esterler) ve lipidler (örneğin, lipofektamin) de tasarlandı.
Genom modifikasyon sistemlerinin, virüsler kullanılmadan, hücreler arası olarak verilmesi için fiziksel yöntemler de geliştirildi: In vitro mikroenjeksiyonlar, ex vivo embriyo veya zigota doğrudan enjeksiyon. Alternatif olarak, elektroporasyon da gen terapi makromoleküllerinin hücre içerisine girebilmesi için hücre zarında geçici gözenekler açmasını sağlamak amacıyla kullanılabiliyor.
Genom düzenleme hem araştırma hem de klinik uygulamalar için muazzam bir olanak sunuyor. Hastalıklara sebep olan mutasyon dizilerinin silinmesi, düzeltilmesi veya terapötik genlerin özel olarak dahil edilmesi yoluyla bir dizi kalıtımsal hastalığı tedavi etme potansiyeline artık kavuşmaya başladık. Gen terapi makromoleküllerinin viral veya viral olmayan yöntemlerle hedef doku ve hücrelere transferinin yanı sıra; programlanabilir nükleazların doğasını ve işlevini anlamamızdaki ilerlemeler de gelecekte ‘tedavi edilemez olan’ kalıtımsal hastalıkları iyileştirmemizde bize muazzam katkılar sağlayacak.
Kaynak: Hao Yin et al. Delivery technologies for genome editing. Nature Reviews. 24 Mart 2017